干细胞治疗:干细胞疗法对糖尿病氧化应激的研究
[本文为疾病百科知识,仅供阅读] 发布日期:2020-02-26 阅读:1,701糖尿病微血管的损伤是糖尿病并发症发生发展的重要因素,近年来发现,氧化应激是损害微血管的重要因素。
因此,减轻微血管氧化应激反应成为防控糖尿病并发症的关键。

什么是氧化应激?
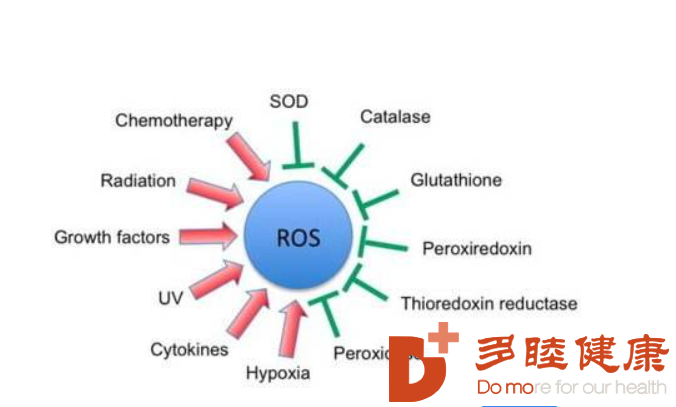
氧化应激是活性氧(ROS)产生和抗氧化防御之间的不均衡所引起的反应,氧化应激在糖尿病微血管病变的发生过程中扮演着重要的角色。
氧化应激可导致微血管炎症浸润,蛋白酶分泌增加,产生大量氧化中间产物,氧化中间产物游走于血管中,影响身体各个部位(例如肾脏、足部、视网膜),因而容易发生糖尿病肾损伤、糖尿病足等。
在糖尿病微血管氧化应激的研究过程中,专家发现干细胞疗法具有抗氧化和抑制炎症的功能,引起了糖尿病领域相关科研人员的重视。
干细胞疗法对糖尿病氧化应激的研究
研究试验:王等人通过实验型糖尿病大鼠进行静脉输注干细胞2.0×105个·kg-1,同时设置模型组和空白组,8周后检测大鼠血清中总抗氧化能力(T-AOC)、超氧化物歧化酶(SOD)、丙二醛(MDA)等氧化应激指标,以及空腹血糖(FPG)、空腹胰岛素水平(Fins)和胰腺组织切片等。
结果显示:经干细胞移植后,大鼠的FPG、Fins及MDA指标降低;T-AOC、SOD指标显著升高,说明干细胞可提高大鼠体内的抗氧化能力,抑制胰腺组织的炎症反应,修复胰岛细胞损伤,有效改善高血糖症状。
干细胞疗法改善糖尿病肾损伤大鼠肾小球损伤
研究试验:微血管应激反应是引起糖尿病肾损伤的重要因素,吕等人将糖尿病肾损伤大鼠分为模型组和干细胞组,干细胞组的大鼠经尾静脉注射干细胞2×106个/500ul2次(间隔1周),8周后观察大鼠的生化指标,进行肾功能评价,并大鼠肾小球膜系细胞(GMC)与干细胞体外培养。
结果显示:经干细胞输注后,降低了糖尿病肾病大鼠的血糖,肾小球纤维化得以缓解,改善肾功能。
干细胞进入肾脏后主要分布于肾小球及血管周围;干细胞组大鼠尿蛋白水平,肾肥大指数和肌酐清除率明显下降;肾脏中SOD活性上调,MDA含量及ROS表达下调,同时,体外实验显示GMC与干细胞共培养组经高糖刺激后氧化应激产物较其他组下调。
干细胞疗法减轻氧化应激并改善糖尿病足
临床试验:以往报道,糖尿病患者足部末端微血管氧化应激状态增强,抗氧化状态减弱。高等人选取30例糖尿病足患者作为干细胞研究对象,进行干细胞移植12周后检查各项生化指标和临床症状。
结果显示:干细胞可降低MDA含量,上调T-AOC,糖尿病受试者的足部疼痛、冷感 、麻木、间歇性跛行具有显著改善。研究人员认为,干细胞可通过抗氧化改善内环境,进而促进侧支循环建立,改善下肢缺血状态。
干细胞减轻微血管应激反应的可能机制
1.旁分泌抑制作用
干细胞通过旁分泌细胞因子改善微血管内环境,抑制微血管的应激反应,降低氧化应激指标,提高氧化应激环境中细胞的正常存活率。
2.减少细胞内糖摄取
干细胞通过降低血糖及减少细胞内糖摄取,并下调TGF-β表达从而下调细胞膜表面GLUT1(葡萄糖转运蛋白)的定位,最终抑制了氧化应激。
3.重建微血管
干细胞具有多向分化的功能,干细胞在体内分化为血管内皮细胞,形成新的毛细血管,促进侧支循环建立,改善和恢复肾脏、下肢等各部位血流。
随着科学家对干细胞的不断探究及临床试验,干细胞疗法或将成为临床医学重要的防控途径,为更多糖尿病患者解除疾病困扰!
推荐阅读:肝癌术后复发率达70%,预防复发和转移应该如何做?
本文链接地址:http://domo-kenkou.com/gxbzs/4663.html